腐食とは?
まず、腐食を理解するためには、学校で習った「イオン化傾向」というものが基になります。
これは、元素をイオンになりやすい順に並べたもので、言い換えれば「酸化しやすい」、「さびやすい」順番ということになります。
卑 ← K,Na,Mg,Al,Zn,Cr,Fe,Ni,Sn,(H),Cu,Ag,Pt,Au → 貴
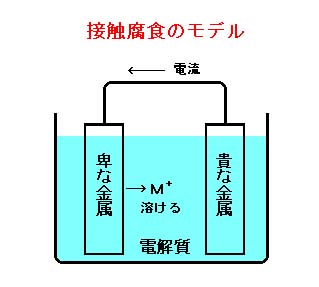
次に、イオン化傾向の異なる2種類の金属を電解質溶液に漬けて、それぞれを導線で結ぶとイオン化傾向の大きな(卑な)金属がイオンとなって溶け出し電流が流れます。これを接触腐食と呼びます。
金属の防食方法
鉄鋼などは単独で腐食しやすいので、防食のため他の金属によるめっきが行われ、カソード型めっきとアノード型めっきの2つに分類することができます。
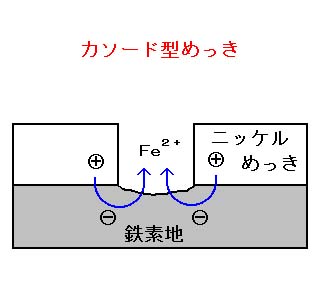
カソード型では、めっき皮膜が素地に対して「貴」ですから、たとえめっき皮膜の耐食性が優れていても、ピンホール等の欠陥部があれば素地金属との間に電流が流れ、素地側が腐食していきます。
従いまして、カソード型のめっきでは、膜厚が十分厚くピンホールのないことが防食の条件となります。
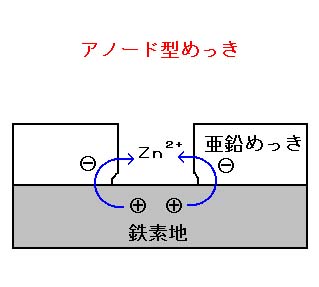
一方、アノード型めっきの代表である亜鉛めっきでは、素地に対して「卑」ですから、ピンホール等を通して素地が露出してもめっき皮膜が犠牲となって溶解し、素地を守ることができます。しかし、亜鉛は大気中で腐食し白錆を生じるので、亜鉛めっきの耐食性向上のためにクロメート処理等で仕上げられます。
また、亜鉛は溶解していくものですから、めっき厚さが耐食性に大きく影響します。
組み合わせ防食法
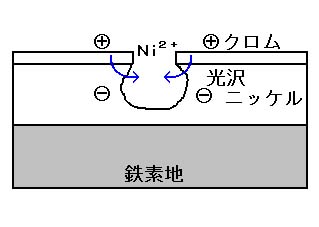
組み合わせ防食の代表的なめっきとして、ニッケル-クロムめっきがあります。クロムはニッケルに対して卑な金属ですから、すぐに腐食しそうに思えますが、実は酸化しやすい金属で不動態化(それ以上さびない状態)する性質から、クロム酸化物はニッケルよりも貴な状態にあるのです。
従いまして、クロムに欠陥があると、まずニッケルが腐食されて鉄素地が露出するまでの間、素地の腐食を防止するという効果があります。
 |
→ |
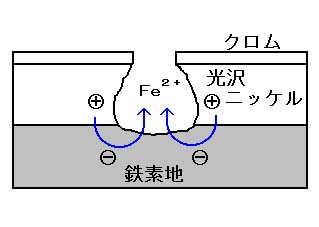 |
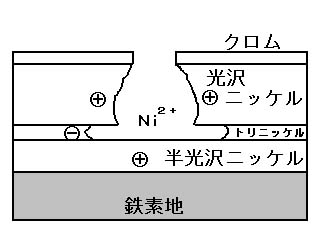
さらに、耐食性の異なるニッケルを2層、3層にめっきし、素地までの到達をずっと遅らせているのが二重ニッケルめっき、三重ニッケルめっきです。
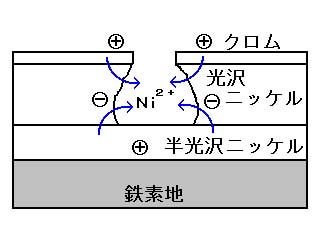
二重ニッケルめっきの場合、クロムと光沢ニッケルの間で腐食が進行しますが、半光沢ニッケルめっきに達するとここでも光沢ニッケルがアノードとなり、光沢ニッケルが腐食します。
このような現象が起こるのは、光沢ニッケルめっきには約0.05%の硫黄が含まれていることから、半光沢ニッケルよりも電位が「卑」となるためです。
三重ニッケルめっきでは、半光沢ニッケルめっきの下にさらに硫黄分の多いトリニッケルめっきを付けることで、腐食はこの層で横に広がり、光沢ニッケルの腐食は少なく耐食性が増加します。
腐食電流分散型防食法
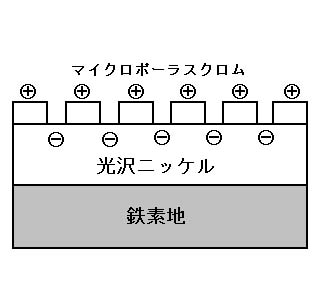
クロムめっきに工夫を凝らし、微細なクラックやピンホールを無数に作ったもので、マイクロポーラスまたはマイクロクラッククロムめっきと呼ばれます。
これは、クロムめっきのクラック数を250/cm以上にすることによりクロムとニッケル間の接触腐食が多くの箇所で起こるので、腐食電流が分散される結果、光沢ニッケルめっきの腐食が小さく、素地に達するまで相当な時間がかかるというものです。
これを二重ニッケルや三重ニッケルと組み合わせれば効果もさらに向上します。